Das musst du wissen
- Das Tübinger Biotech-Unternehmen Curevac wurde im Jahr 2000 gegründet.
- Es entwickelte die mRNA-Technologie, die heute von Herstellern von Impfstoffen gegen Covid-19 wie genutzt wird.
- Curevacs eigener Covid-19-Impfstoff zeigte in den klinischen Studien eine geringe Wirksamkeit von unter fünfzig Prozent.
Wer hätte gedacht, dass das überraschende Ausscheiden der deutschen Mannschaft gegen Kroatien bei der Fussballweltmeisterschaft 1998 eine Begegnung auslösen würde, die zur Gründung des ersten RNA-Impfstoffunternehmens Curevac führen würde? In jenem Sommer, als die Mannschaft ausgeschieden war, richtete der deutsche Biologe Ingmar Hoerr seine Aufmerksamkeit auf die französische Mannschaft, Les Bleus. Und da sich in seiner Forschungsgruppe an der Universität Tübingen ein junger französischer Forscher befand, freundeten sie sich an und arbeiteten dann auch zusammen.
Doch von Anfang an: Nach seinem Studium an der Ecole Normale Supérieure in Paris kam der Franzose Steve Pascolo in die kleine Universitätsstadt in Baden-Württemberg, um in der Gruppe des Immunologen Hans-Georg Rammensee zu promovieren. Der deutsche Professor ist ein führender Forscher auf dem Gebiet der T-Zellen, den weissen Blutkörperchen, die kontaminierte Zellen oder Krebszellen angreifen.
Vom Fussball zu den Lymphozyten
Hans-Georg Rammensee entwickelt Impfstoffe, die diese T-Lymphozyten so aktivieren können, dass sie Krebs zerstören. Er ist für sehr unterschiedliche Ansätze offen und verfolgt die Idee, die natürlichen Abwehrmechanismen zu aktivieren, die uns ein Leben lang vor der Entstehung von Tumoren schützen. Es sei denn, der Krebs ist in der Lage, diese Immunabwehr irgendwie ausser Kraft zu setzen oder zu umgehen.
Steve Pascolo will die vielen von Hans-Georg Rammensee entwickelten Impfstoffe an den transgenen Mäusen testen, die er im Rahmen seiner Diplomarbeit am Pasteur-Institut geschaffen hat. Unter der Leitung von François Lemmonier erfand er neue Tiermodelle. Seine Mäuse enthalten Gene menschlichen Ursprungs, die humanisierte T-Lymphozyten erzeugen. Natürlich fasziniert ihn, was ihm Ingmar Hoerr zwischen zwei Fussballspielen erzählt.
Eine natürliche Technologie
Auf einer Konferenz in Israel im Februar 1996 entdeckte Hans-Georg Rammensee Pionier-Arbeiten zur mRNA, die ihm einen neuen Weg für seine Impfstoffprojekte eröffneten. Eli Gilboa, Professor an der Duke University, extrahierte dendritische Zellen, also Zellen, die eine Vorläuferrolle bei der Immunantwort spielen, und übertrug in vitro mRNA auf sie.
In diesen Zellen dienen die Informationen der RNAs als Gedächtnis für Proteine, die für Krebs charakteristisch sind, um diese zu identifizieren und anzugreifen. Einmal in den Körper zurück injiziert, lösen diese dendritischen Zellen die Produktion von T-Lymphozyten aus. Genau wie bei einem Impfstoff. Solche Überlegungen machte sich Drew Weissman in den Vereinigten Staaten fast zur selben Zeit. Das erklärt sein Interesse für Kati Karikós Forschung, zwei Jahre später (siehe Folge 4).


Die Universität von Tübingen.
Eine aufwändige Methode
«Zu dieser Zeit arbeitete ich an Krebsimpfstoffen, hauptsächlich auf der Basis von kleinen Proteinen, sogenannten Peptiden, die in Krebszellen identifiziert wurden. Aber es gab noch viele Herausforderungen und ich war an allen Ansätzen interessiert», sagt Hans-Georg Rammensee in einer Videokonferenz mit Heidi.news aus seinem Büro. «Die von Eli Gilboa vorgestellte Methode war recht aufwändig, da die Zellen extrahiert, mit mRNA mit der nötigen Information versehen und dann neu injiziert werden mussten. Ich fragte mich also, was passieren würde, wenn wir die mRNAs direkt in den Körper injizieren würden.»
Nach seiner Rückkehr nach Deutschland beantwortete Ingmar Hoerr diese Frage im Rahmen seiner Diplomarbeit. Wie in den Experimenten, die in den USA von Robert Malone, Phil Felgner und Jon Wolff durchgeführt wurden (siehe Folge 2), injizierte er zunächst nackte mRNAs, aber auch solche, die in Liposomen oder in Peptiden verkapselt waren, in die Ohren von Mäusen. In allen Fällen wurden die Proteine exprimiert. Ironischerweise glaubte Ingmar Hoerr zunächst, wie schon 1990 die Forscher an der University of Wisconsin in Madison, dass er seine Ergebnisse verwechselt hatte. Denn die nackten RNAs zeigten eine bessere Expression als die verkapselten. Seine Ergebnisse wurden im Jahr 2000 im European Journal of Immunology veröffentlicht.
Die höhere Wirksamkeit dieser nackten RNAs ist wichtig. Sie führte zur Entwicklung einer anderen Technologie als derjenigen, die heute von Biontech/Pfizer und Moderna bei mRNA-Impfstoffen gegen Covid-19 eingesetzt wird. Diese Firmen nutzten RNAs mit einer von Kati Karikó und Drew Weissman modifizierten Base (Uridin, siehe Folge 4). Die Tübinger Forscher hingegen verwendeten nicht dieses Pseudo-Uridin, um die vom Immunsystem erzeugte Entzündung zu reduzieren, sondern andere Techniken.
Die Mauer der Skepsis
Im Sommer 1998, als Zinédine Zidane zwei der drei Tore im triumphalen Finale gegen Brasilien schoss und die Zusammenarbeit zwischen Steve Pascolo und Ingmar Hoerr begann, waren die Impfstoffe noch in weiter Ferne. «Wir dachten, dies sei der Weg, um Impfstoffe herzustellen, die viel sicherer sind als DNA-Impfstoffe», erklärt Steve Pascolo, heute Leiter des Dermatologie-Labors am Universitätsspital Zürich. «Denn im Gegensatz zur DNA ist die RNA vergänglich und geht nicht in den Zellkern. Damit ist jede Möglichkeit der Integration in das Genom des Empfängers ausgeschlossen.»


Das Gründungsteam von Curevac.
Sie beginnen, es an Mäusen auszuprobieren, die als Modelle für Melanome modifiziert waren. Dann erweiterten sie ihre Versuche nicht nur an Mausmodellen mit Krebs, sondern auch mit Infektionskrankheiten wie HIV, Hepatitis B und humanen Papillomviren. «Es hat funktioniert, auch wenn die Immunantwort nicht sehr stark war», erinnert sich Hans-Georg Rammensee. «Es war vielversprechend, aber wir stiessen bald auf eine Mauer der Skepsis.»
Steve Pascolo erklärt weiter. «Mit unseren mRNAs waren wir in der Lage T-Zellen zu erzeugen, aber das hat niemanden interessiert. Wenn ich unsere Ergebnisse auf Konferenzen präsentierte, gab es keine Fragen. Das ging so weit, dass ich ein paar Folien aus meiner Präsentation herausgenommen habe, um mir selbst Fragen zu stellen.» Ingmar Hoerr, der in die Pharmaindustrie einsteigen wollte, stiess bei seinen Vorstellungsgesprächen auf die gleiche Ungläubigkeit. Da sie schliesslich niemand haben wollte, beschlossen sie, ihre eigene Firma zu gründen.


Das erste Labor, dass in einer Ecke am Department Chemie der Universität eingerichtet wurde.
Das erste RNA-Startup
Curevac wurde im Jahr 2000 gegründet, nachdem die Universität Tübingen ein Patent auf einen mRNA-Impfstoff angemeldet hatte. Geforscht wurde mit nackter RNA, doch die Option der Verkapselung wurde nicht aufgegeben. Wegen der Pionierarbeit von Frédéric Martinon und Pierre Meulien am Cochin-Institut (siehe Folge 3) war es damals unmöglich, ein Patent auf die Verkapselung in Liposomen anzumelden. Das Patent wurde deshalb auf eine Verkapselung mit Peptiden, Protamin, aus dem Chemielabor von Gunther Jung an der Universität Tübingen angemeldet. Auf diesem Gebiet wird weiterhin geforscht, aber nicht im gleichen Ausmass wie über Lipid-Nanopartikel.
Das Gründungsteam von Curevac, Ingmar Hoerr, der ein MBA gemacht hat, und Steve Pascolo, als Chief Scientific Officer, wurde mit dem Biochemiker Florian Von der Mülbe verstärkt, der damals seine Position bei Roche aufgab. Sie erhalten zunächst 100 000 Euro von einem schottischen Investor, der sich aber plötzlich zurückzieht und die Rückzahlung verlangt. Da sie einen Teil des Geldes ausgegeben hatten, wurden sie in letzter Minute vor der Insolvenz gerettet, indem sie einen Kredit von 20 000 Euro bei der kleinen Sparkasse in Tübingen aufnahmen.
800 Euro pro Monat
Das Land Baden-Württemberg wollte seinem Nachbarn Bayern in der Biotechnologie Konkurrenz machen und unterstützte das kleine Team mit dem Förderprogramm «Junge Innovatoren». Sie erhielten ein kleines, renoviertes Labor im Departement Chemie. Ingmar Hoerr und Florian Van der Mülbe müssen mit einem mageren Gehalt von 800 Euro pro Monat auskommen. Steve Pascolo verdient mit universitären Forschungsprogrammen kaum doppelt so viel.


Als Curevac ein Start-up war, gab es Pizza.
Abgesehen von den Gehältern wurde die Geldfrage für die drei angehenden Unternehmer rasch eine harte Realität. Um die Investoren zu überzeugen, mussten sie klinische Studien durchführen. Im Jahr 2001 erhielten sie eine europäische Finanzierung, um eine Studie über die Schweinegrippe durchzuführen. Da es sich hier aber um Tiermedizin handelte, war dies nicht sehr profitabel. Was sie benötigten war eine klinische Studie am Menschen. Dies wiederum bedingte Einrichtungen, die den Standards der Pharmaindustrie, der sogenannten Good Manufacturing Practice GMP, entsprechen.
Diesen Standard zu erreichen, ist für ein Start-up-Unternehmen eine gewaltige Aufgabe. Doch dann baute das Team 2003 das erste Instrument für eine industrielle Produktion von mRNA. Noch im selben Jahr erhielt Curevac schliesslich 2,7 Millionen Euro von einem Mannheimer Risikokapitalgeber. Das gab ihnen Aufwind. Das Unternehmen zog kurz darauf in den Technologiepark Tübingen. Die kleine Stadt, in der ein Drittel der Einwohnerschaft Studentinnen und Studenten sind, denkt gross. Es hat fünf Millionen Euro in brandneue Laboratorien investiert, die den GMP-Standards entsprechen. Curevac mietet sich ein und kann mit der eigentlichen Arbeit beginnen.
Menschenversuche sind im deutschen Medizinrecht vorbildlich streng. Aber einer seiner Paragrafen erlaubt es einem Arzt immer noch, jede Substanz an einem Patienten zu testen. Vorausgesetzt, er produziert sie selbst. Steve Pascolo und Ingmar Hoerr sehen darin die Möglichkeit, in Zusammenarbeit mit Dermatologen des Universitätsspitals, die mRNA herstellen werden, eine erste klinische Studie zu Melanomen zu starten.
Der erste mit RNA geimpfte Mensch
Um sich zu vergewissern, dass die Technologie sicher ist und funktioniert, schlägt Ingmar Hoerr vor, sie an einem ersten Probanden auszuprobieren. Steve Pascolo bat dann einen der Dermatologen, Benjamin Weide, ihm mRNAs ins Bein zu spritzen, die lumineszierende und somit leicht sichtbare Kontrollproteine kodieren. Im Jahr 2003 war er der erste Mensch, der in vitro synthetisierte mRNA erhielt.


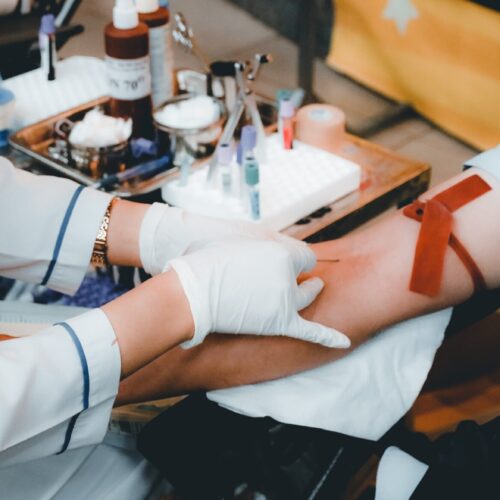
Biopsie am Bein von Steve Pascolo, der erste mit RNA geimpfte Mensch.
Die ersten klinischen Studien begannen mit einigen wenigen Patienten mit Melanomen und Nierenkrebs, deren Therapiemöglichkeiten ausgeschöpft waren. Doch trotz ermutigender Ergebnisse für eine so neue Technologie wurden ihre Veröffentlichungen von den grossen Fachzeitschriften abgelehnt. Die erste Studie erschien erst fünf Jahre später, im Jahr 2008, im Journal of Immunotherapy.
Diese Versuche werden jedoch mehrere Auswirkungen haben. Zum einen erregten sie die Aufmerksamkeit eines einflussreichen Biotech-Unternehmers in Deutschland: Friedrich von Bohlen und Halbach. Als Mitglied der Familie Krupp und Absolvent der ETH Zürich war er 1997 Mitbegründer des Bioinformatik-Unternehmens Lion Biosciences. Nach dem Börsengang im Jahr 2000 wurde es zu einer Erfolgsgeschichte.
Milliardär willkommen
Er stellt die Gründer von Curevac dem Milliardär Dietmar Hopp vor, der den deutschen IT-Riesen SAP gegründet hat. Als Informatiker gefällt ihm der Ansatz von Curevac, molekulare Informationen zu übertragen und dabei die DNA-Etappe zu überspringen. Ende 2005 investierte Dietmar Hopp über seinen Venture-Capital-Fonds 35 Millionen Euro in Curevac.


Hauptsitz des Unternehmens im Technopark von Tübingen.
Für das Unternehmen war es eine Renaissance. Doch Steve Pascolo sieht darin eher einen Wendepunkt. Auf Bitten von Friedrich von Bohlen und Halbach hat er sich bereit erklärt, noch ein Jahr bei Curevac zu bleiben, doch seine Interessen haben sich nach Zürich verlagert, zu seinem Universitätsspital und einem Pionierforscher: Thomas M. Kündig. «Er ist der Vater der intralymphatischen Impfung», erklärt er. «Da sich in den Lymphknoten die meisten an der Immunantwort beteiligten Zellen befinden, dachte ich, es wäre interessant, etwas anderes als unsere intradermalen RNA-Injektionen zu versuchen, um antigene Proteine zu produzieren, die ohnehin zu diesen Lymphknoten gehen müssen, um T-Zellen zu stimulieren.»
Krebs – eine grosse Sache
Er baut mit dem Zürcher Team eine RNA-Impfstoffstudie für Lungenkrebs auf. Dies brachte ihn zurück in die akademische Welt, wo er bis heute ist. Doch in Tübingen wird sein Abgang bedauert.
Mitte der 2000er-Jahre interessierte sich niemand für Impfstoffe gegen Infektionskrankheiten. Das grosse Geschäft war Krebs. Die Investoren interessierten sich nur für das Versprechen der sogenannten Immuno-Onkologie. Die Pharmakonzerne begannen hunderte von monoklonalen Antikörpern zu entwickeln. Allerdings werden diese Antikörper, mit denen inzwischen Milliarden verdient werden, ex vivo von gentechnisch veränderten Zellen produziert. Es spricht jedoch nichts dagegen, dass sie in vivo von patienteneigenen Zellen produziert werden. Theoretisch würde es reichen, die Baupläne dieser Proteine in mRNAs, zu schicken, damit die Zellen sie dort produzieren, wo sie nützlich sind.
Steve Pascolo kam auf die Idee solcher sogenannter therapeutischer mRNAs, als er bemerkte, dass ein Forscher aus der Gruppe von Hans-Georg Rammensee Schwierigkeiten hatte, eine elaborierte, sogenannte bispezifische, Form herzustellen. Er entwickelte diese Technologie bei Curevac, doch seine Nähe zu Zürich führte dazu, dass ihm das von einer Geheimhaltungskultur geprägte Unternehmen die Tür verschloss. Er musste darum kämpfen, dass sein Name auf dem Patent steht, das 2007 für diese Technologie angemeldet wurde. Das verhinderte nicht, dass das 2016 endlich genehmigte Patent sofort von nicht weniger als sieben Anwaltskanzleien angegriffen wurde und diese seine Ungültigkeit erwirkten.
Kleinste Schritte
Curevac hat zu der Zeit jedoch ein anderes Problem. Da das Unternehmen zunächst mit nackten RNAs arbeitete, bestand die Herausforderung darin, den Anteil zu verbessern, der tatsächlich von den Zellen aufgenommen und in Proteine umgeschrieben wird. Der einfachste Weg ist, die Dosierung zu erhöhen, also mehr mRNA zu spritzen. In den 2000er-Jahren wurden bis zu 800 Mikrogramm pro Injektion verwendet, das ist das achtzigfache der Menge, die im Covid-Impfstoff von Curevac enthalten ist. Im Hinblick auf die geringe Wirksamkeit von knapp fünfzig Prozent in den klinischen Studien, deren Ergebnisse die Firma Juni 2021 bekannt gab, wurde der Impfstoff dagegen möglicherweise zu konservativ dosiert.
_____________
Abonniere hier unseren Newsletter! ✉️
_____________
Curevac hat keine Lizenz für die von Kati Karikó und Drew Weissman an der Universität von Pennsylvania entwickelte Technologie zur Basenmodifikation von mRNAs. Sie wird daher andere Wege zur Verbesserung ihrer Technologie entwickeln Angesichts der enttäuschenden Ergebnisse der Covid-Impfstoffversuche bestehen jedoch nach wie vor gewisse Zweifel.
In der mRNA gibt es kodierende und nicht-kodierende Bereiche. Letztere sind aber für ihre Stabilität und ihre Fähigkeit, sich an Ribosomen zu binden, wichtig. Curevac begann mit der Optimierung dieser Bereiche. Ihre Boten-RNAs sind auch mit einigen der vier Nukleinbasen der RNA, Guanin und Cytosin, angereichert, um die Anzahl derjenigen Basen, insbesondere des Uridins, zu reduzieren, die die angeborene Immunantwort auslösen.
Verbesserung der RNA-Kappe
Die Methode wurde «GC rich» getauft und 2002 von der Firma patentiert. Sie verbessert die Effizienz der Übersetzung von mRNA in Proteine. Allerdings werden dadurch Entzündungsreaktionen nicht vollständig ausgeschaltet, da zehn der zwanzig Aminosäuren, aus denen Proteine aufgebaut sind, Uridin oder Pseudo-Uridin benötigen, um exprimiert zu werden. Die Forscher des Unternehmens optimieren auch die Codons, die Wörter, die jede Aminosäure in der RNA-Sequenz kodieren. Das erlaubt, Proteine in einigen dieser Aminosäuren anzureichern und diese lösen so eine bessere Antwort des Immunsystem aus.
Andere Forschungen zielen darauf ab, die Kappe der Boten-RNAs zu verbessern, ihre charakteristische Extremität so zu sagen. Diese ermöglicht es den Ribosomen, den Proteinfabriken, sie zu identifizieren. Die Herausforderung besteht hier darin, sicherzustellen, dass alle RNAs eine Kappe tragen. Sie müssen eine Extremität haben, die es den Ribosomen ermöglicht, die mRNAs in der Zelle zu identifizieren. Dies ist allerdings bei ihrer Synthese noch lange nicht der Fall. Ausserdem müssen diese künstlichen Kappen so optimiert werden, dass sie gut an den Ribosomen haften.
In diesem Bereich muss Curevac wie seine Konkurrenten noch bis 2017 und auf die Entwicklung einer solchen Kappe durch die kalifornische Firma Trilink warten. Diese erfasst bei ihrer Herstellung jede RNA und die Ribosomen erkennen sie zu hundert Prozent. «Das ist ein riesiger Sprung, im Vergleich zu den Babyschritten, die wir in den letzten zwanzig Jahren gemacht haben», sagt Steve Pascolo.
Das Ergebnis dieser verschiedenen Verbesserungen ist eine mRNA, die stabiler ist und mehr Proteine bilden wird. Für Curevac ist der Nachweis dieser Wirksamkeit jedoch noch durch die enttäuschenden Ergebnisse der Covid-Impfstoff-Studien beeinträchtigt. Unklar ist, ob dies an der niedrigen Dosierung liegt oder daran, dass Curevac nicht das Pseudo-Uridin von Karikó und Weissman verwendet. Wie auch immer, bisher hat noch keiner der Impfstoffe von Curevac die Zulassung erhalten.
DARPA lässt Impfstoffe wieder aufleben
Das Unternehmen hatte sich lange Zeit auf Krebsimpfstoffe konzentriert. Ein Bereich, in dem es viele Enttäuschungen gab, wie das Scheitern des am weitesten fortgeschrittenen Programms gegen Prostatakrebs im Jahr 2017 zeigte. Für Curevac hat sich jedoch im Laufe der 2010er-Jahre ein weiteres, von der Pharmaforschung weitgehend vernachlässigtes Feld aufgetan.


Curevac konnte dank dem erneuten Interesse an Impfstoffen sein industrielles Instrument bauen.
Die Forschung für Impfstoffe gegen Infektionskrankheiten wurde – mangels erfolgsversprechender Ergebnisse – weitgehend aufgegeben. Doch im Jahr 2011 hat in den USA die Defense Advanced Research Projects Agency (DARPA) ein umfangreiches Programm gegen Infektionskrankheiten gestartet. Dies wird mit den Risiken der bakteriologischen Kriegsführung oder des Bioterrorismus begründet. In diesem Rahmen führt Curevac gemeinsam mit Sanofi Pasteur ein Impfstoffentwicklungsprogramm gegen Infektionskrankheiten – deren Namen nicht bekannt gegeben wurden – durch, das mit 33,1 Millionen Euro dotiert ist.


Von Tesla entwickelter RNA-Drucker.
Beim Einstieg in den Bereich der Infektionskrankheiten arbeitet Curevac mit Johnson & Johnson an der Entwicklung eines RNA-Grippeimpfstoffs und daraufhin gibt es 2015 von der Gates Foundation Unterstützung für verschiedene Impfstoffe. Auf dieser Basis startet Curevac 2017 eine erste klinische Studie für einen Tollwut-Impfstoff. Ihre noch unvollständigen Ergebnisse werden hinterfragt. Um Toxizitätsprobleme zu vermeiden, war nämlich eine besonders niedrige Dosierung von einem Mikrogramm erforderlich. Aber wenn die Dosierung eines RNA-Impfstoffs so weit reduziert wird, besteht die Gefahr, dass er keine therapeutische Wirkung hat.
Die Erfahrungen aus diesen Programmen haben aber ein industrielles Instrument geschaffen, das Curevac einen Vorsprung für die Covid-Impfstoffe verschafft hätte und auch für andere Impfstoffe interessant bleibt. Und es machte auch Fortschritte an einer anderen kritischen Front, mit denen es bisher weniger arbeitete: Lipid-Nanopartikel.
Im Rahmen der Zusammenarbeit mit Sanofi arbeitet Curevac mit einem kleinen französischen Start-up namens In-Cell-Art zusammen, das Lipid-Nanopartikel entwickelt. Diese Zusammenarbeit wird zurzeit noch ausgewertet. Doch für seinen Impfstoff Covid-19 hat sich Curevac, wie auch Biontech, für eine Zusammenarbeit mit dem kanadischen Unternehmen Acuitas entschieden.
mRNA-Drucker
Mit den enttäuschenden Ergebnissen seines Covid-Impfstoffs konnte Curevac nicht aus seinem Schildkrötenpanzer herauskommen. Aber das Unternehmen hat noch andere Karten im Ärmel. Seine Impfstofftechnologie ist preiswerter und muss nicht bei so kalten Temperaturen gekühlt werden wie die von Biontech/Pfizer und Moderna. Es arbeitet an RNA-Impfstoffen, zum Beispiel gegen Gelbfieber oder Malaria, die für die Verteilung in Entwicklungsländern geeignet wären.
Ausserdem entwickelt Curevac in Zusammenarbeit mit Tesla mRNA-Drucker. Es sind kleine Produktionseinheiten, die leicht dezentralisiert werden können, um Medikamente nach Bedarf und massgeschneidert für einzelne Patienten zu produzieren. Dies könnte einer der Schlüssel sein, um mRNA-Technologien auf Krankheiten anzuwenden, die nicht viral sind. Doch die klinischen Tests lassen noch auf sich warten.
Nächste Folge: Modernas Griff nach den Sternen
Alle Folgen:
Heidi.news